식품의약품안전처는 위장약 ‘잔탁’과 잔탁에 사용하는 원료제조소에서 생산된 라니티딘을 검사한 결과 N-니트로소디메틸아민(NDMA)이 검출되지 않았다고 16일 밝혔다.
식약처는 미국 식품의약국(FDA)와 유럽의약품청(EMA)이 글락소스미스클라인(GSK)의 잔탁에서 NDMA가 검출된 것을 확인했다는 위해정보를 14일 입수했다. NDMA는 세계보건기구(WHO) 국제 암연구소(IARC)가 인간에게 발암물질로 작용할 가능성이 있다고 지정한 물질이다.
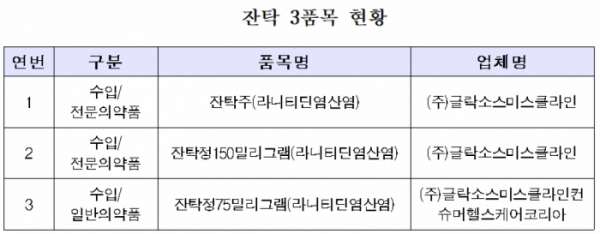
우선 식약처는 FDA가 미량 검출됐다고 발표한 라니티딘 제품 중 한국 GSK가 허가 받은 잔탁 3개품목 29개제품과 잔탁에 사용된 원료 라니티딘(6개), 총 35개를 긴급 수거·검사했다. 검사는 현재 수입 또는 국내 제조되는 모든 라니티딘 원료와 해당 원료를 사용한 의약품(395품목)을 대상으로 확대할 예정이다.
식약처 관계자는 “각국의 NDMA검출 정보를 공유하고 라니티딘 중 NDMA 발생원인 등을 밝히기 위해 미국 FDA와 유럽 EMA 등 각 국 규제기관과 긴밀히 협력하고 있다”며 “FDA 및 유럽 EMA에서는 일부 라니티딘 함유 제제에서 낮은 수준의 NDMA가 검출되었기 때문에 회수 등 조치는 하고 있지 않은 상황이며, 지속적으로 안전성을 조사할 예정이라고 밝힌 바 있다”고 설명했다.
라니티딘은 위산과다, 속쓰림, 위·십이지장궤양, 역류성식도염 등에 사용하는 의약품이다. 지난해 수입 및 생산실적 기준 위장병(소화성궤양) 치료제는 약 1조511억 원이며, 이 중 라니티딘 함유 의약품은 2664억원으로 25.3%에 해당한다. 국내 허가·등록된 라니티딘 원료의약품 제조소는 11곳이다.











![[찐코노미] 테슬라, 진정한 성장 시작되나…국내 자율주행 기술 수준은?](https://img.etoday.co.kr/crop/320/200/2098264.jpg)