식품의약품안전처가 제네릭의약품의 불순물을 사전에 파악하는 등 안전관리 수준을 강화하고, 정보 제공을 확대한다.
식약처는 '제네릭의약품 국제경쟁력 강화를 위한 민관협의체' 운영 결과 이 같은 내용을 포함한 21개 과제를 도출했다고 16일 밝혔다.
우선 식약처는 제네릭의약품의 품질신뢰성을 높이기 위해 전 공정을 위탁 제조해도 GMP 적격성 여부를 사전에 확인하고 허가하기로 했다.
또한, 제네릭의약품의 허가 이후 품질 및 약효에 영향을 미칠 수 있는 세부공정 변경, 원료의 입자크기 변경 등 업체 자율적으로 관리하던 '제조방법'에 대한 변경을 품질·약효 영향에 따라 변경 정도를 차등화하여 사전 변경허가 하는 체계로 강화한다.
주성분과 제형이 같고 함량이 다른 의약품의 첨가제 종류·배합비율이 다를 경우에는 비교용출시험 대신 '생물학적동등성시험'으로 동등성을 입증해야 한다.
특히 N-니트로소디메틸아민(NDMA) 등 불순물 사태를 사전에 방지하기 위해 완제의약품 심사 시 원료의약품에 관한 품질심사를 병행하고, 원료의약품 관련 불순물과 같은 위험요인을 파악하기로 했다.
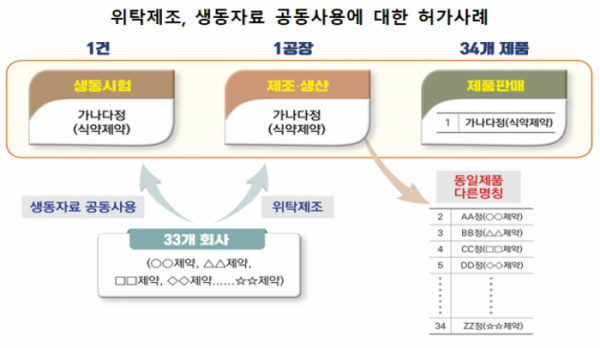
제네릭의약품 관련 정보 제공을 확대하기 위해 식약처는 '제네릭의약품 묶음정보'를 개발, 식약처 홈페이지와 모바일웹 등을 통해 제공할 계획이다. 이 정보는 국내 모든 의약품의 제품개발, 허가심사, 품질관리, 회수·폐기 등의 안전관리 및 안전사용을 위해 활용된다.
현재 단일성분의 의약품만 제품명에 유효성분을 기재하고 있으나, 앞으로는 제품을 쉽게 구분할 수 있도록 복합성분 의약품도 제품명에 유효성분을 함께 기재해야 한다. 이와 함께 제품 외부포장에 제조소·동등성 등에 대한 정보를 표시하는 방안 등을 추진한다.
식약처는 국내 제약사들의 제네릭의약품 개발을 활성화하기 위해 맞춤형 허가 가이드라인을 마련하고 등재된 특허가 없거나 제네릭의약품이 출시되지 않은 제품의 개발을 위한 특허-허가 연계 종합정보를 지속적으로 분석·공개할 예정이다. 아울러 위탁으로 품목허가를 받은 품목은 우선판매품목허가 대상에서 제외하기로 했다.
국내 제네릭의약품의 글로벌 경쟁력을 강화하기 위해 국산 원료의약품 사용 시 완제의약품을 신속히 심사하는 혜택을 제공하고, 해외 주요국과 상호인정협정(MRA)도 지속해서 추진한다.
김영옥 식약처 의약품안전국장은 "의사·약사, 소비자단체 및 제약업계 등과 긴밀히 소통해 정책들이 원활히 추진될 수 있도록 할 것"이라며 "우리나라 제네릭의약품의 품질과 약효가 오리지널 의약품과 같은 수준이 될 수 있도록 안심사용체계를 확립하고 경쟁력 강화를 위해 지원해 나가겠다"고 말했다.











![[정치대학] 美 대선, 막판까지 초박빙…당선자별 韓 영향은?](https://img.etoday.co.kr/crop/320/200/2098110.jpg)