국내 바이오시밀러(바이오의약품 복제약) 산업이 올해 퀀텀점프(대약진)의 발판을 다지고 있다. 셀트리온의 승승장구를 지켜 본 기존 상위 제약업체들이 바이오시밀러 개발에 앞다퉈 속도를 내고 있으며 오리지널 바이오의약품의 대거 특허 만료, 미국의 약가 인하 정책 등 시장 분위기에 편승해 국내 바이오시밀러 업계가 들썩이고 있다.
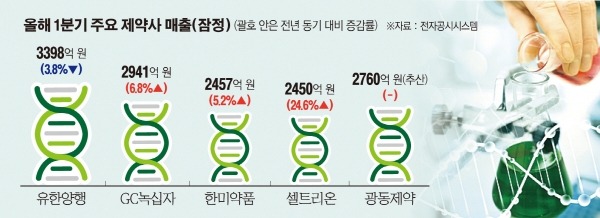
15일 업계와 금융감독원 전자공시시스템에 따르면 셀트리온은 제약업계 매출 기준 TOP3 자리를 위협하고 있다. 셀트리온은 올 1분기 연결기준으로 2450억 원의 매출을 올려 1위 유한양행(3398억 원), GC녹십자(2941억 원), 한미약품(2457억 원)에 이어 제약업계 매출 4위를 기록했다. 아직 실적이 발표되지 않은 광동제약(증권가 추산 매출 약 2760억 원)을 감안하더라도 빅5 제약사 자리를 굳건히 지키게 되는 셈이다. 특히 셀트리온은 24.6%의 매출 성장률을 기록해 유한양행(-3.8%), 녹십자(6.8%), 한미약품(5.2%)에 비해 성장세가 두드러졌다.
셀트리온 관계자는 “1분기는 인플루엔자(독감) 항체 신약 ‘CT-P27’의 임상 비용과 혈액암 치료용 바이오시밀러 ‘트룩시마’, 유방암·위암 치료용 바이오시밀러 ‘허쥬마’의 특허 소송비용 등으로 인해 판매관리비가 증가했음에도 자가면역질환 바이오시밀러 ‘램시마’의 지속적인 유럽 및 미국시장 점유율 확대와 트룩시마의 매출 성장으로 호실적을 거뒀다”며 “앞으로도 유럽에서 바이오시밀러 3개 제품(램시마, 트룩시마, 허쥬마)을 통한 시장 공략을 본격화할 것”이라고 말했다. 현재 유럽 시장에서 오리지널(레미케이드) 시장의 50% 이상을 대체하고 있는 램시마(미국 제품명:인플렉트라)의 경우 미국에서도 올 1분기 작년 같은 기간보다 224% 늘어난 5500만 달러(약 590억 원)의 매출을 기록하며 ‘돌풍 성장’의 주역이 됐다.
세계 최초 항체 바이오시밀러인 ‘램시마’를 개발하며 전통적인 합성의약품이 아닌 바이오시밀러로 승부를 낸 셀트리온의 비약적인 성장은 한국 바이오시밀러 시장 확대의 긍정적인 ‘트리거(방아쇠)’로 작용하고 있다. 삼성바이오로직스의 자회사이자 바이오의약품 연구개발(R&D)을 담당하고 있는 삼성바이오에피스도 총 6개의 바이오시밀러 파이프라인 중 5개가 국내를 비롯해 의약 선진시장인 유럽에서 허가를 받으며 시장에 안착, 국내 제약업계의 시선을 끈 성공 사례로 꼽힌다.
국내 제약업계에서는 동아에스티, 종근당, 일동제약, LG화학, CJ헬스케어 등이 셀트리온과 삼성바이오에피스의 뒤를 이어 한국형 바이오시밀러 개발에 가속페달을 밟고 있다. 이들 업체는 기존 류머티즘 관절염 등 자가면역질환이나 항암 치료제 위주에서 당뇨병, 황반변성, 빈혈, 건선 치료제 등 타깃 질환으로도 확대 중이다.
특히 2015년 11월 특허가 만료된 미국 얌젠의 빈혈치료제 ‘네스프’의 첫 바이오시밀러를 개발하기 위한 경쟁이 뜨겁다. 종근당은 지난해 12월 식품의약품안전처에 네스프 바이오시밀러 ‘CKD-11101’의 허가를 신청했으며 승인되면 내년 세계 최초 네스프 바이오시밀러로 출시될 예정이다. 지난달 말에는 구조가 복잡해 정제가 어려운 주성분 ‘다베포에틴 알파’를 높은 순도로 정제하는 제조법에 관한 미국 특허를 취득, 해외시장 진출에 가속도를 내겠다는 계획을 밝히기도 했다. 동아에스티도 메이지홀딩스와 일본에서 바이오시밀러 전문업체 디엠바이오를 설립하고 네스프 바이오시밀러인 ‘DA-3880’ 3상을 공동 진행하고 있으며 CJ헬스케어 역시 지난해 초 식약처로부터 네스프 바이오시밀러 CJ-40001의 3상을 승인받아 안전성과 유효성 시험에 나섰다.
한국노바티스의 망막질환 치료제 ‘루센티스’의 바이오시밀러 개발도 한창이다. 종근당은 바이오시밀러 ‘CKD-701’의 전임상을 진행 중이며, CJ헬스케어와 동아에스티도 후보물질의 기술 수출을 목표로 개발에 속도를 내고 있다. 일동제약의 경우 최근 루센티스 바이오베터 ‘IDB0062’의 국내 조성물 특허를 취득했다.
이 밖에도 LG화학은 올해 3월 식약처로부터 자체 개발 첫 바이오시밀러 제품인 ‘유셉트(오리지널 의약품: 자가면역질환 치료제 엔브렐)’의 판매 허가를 획득하고 셀트리온과 삼성바이오에피스가 양강체제를 형성해온 자가면역질환 바이오시밀러 시장에 본격 출사표를 던졌다. 업계 관계자는 “2022년까지 주요 오리지널 바이오 의약품 약 28개의 특허 만료가 예상된다”면서 “글로벌 바이오시밀러 시장을 선점하기 위한 국내 후발주자들의 발걸음은 더욱 빨라질 것”이라고 말했다.
바이오시밀러는 기존 바이오 신약과 비교해 동등한 효능을 보이지만 개발 비용과 기간을 줄일 수 있어 경제성이 큰 의약품으로 인식된다. 의약품전문 조사업체 프로스트앤설리반에 따르면 글로벌 바이오시밀러 시장 규모는 2013년 9억 달러(9596억 원)에서 2020년 304억 달러(약 33조 원), 2025년 663억 달러(약 71조 원)로 성장할 것으로 추산된다. 최근 도널드 트럼프 미국 대통령이 ‘바이오시밀러 장려’를 포함한 약가 인하 정책을 발표한 점도 앞으로의 시장 전망성을 밝히고 있다. 유럽에 비해 상대적으로 보수적이었던 미국 바이오시밀러 시장 진입의 문턱이 낮아질 것으로 전망되기 때문이다. 당장 셀트리온의 트룩시마와 허쥬마의 연내 미국 식품의약국(FDA) 허가에 청신호가 켜질 것으로 보인다. 신재훈 이베스트투자증권 연구원은 “트럼프 대통령의 청사진은 바이오시밀러와 제네릭을 장려해 가격경쟁을 확대하겠다는 것”이라며 “국내 업체 중 셀트리온이 미국 바이오시밀러 장려 정책에 가장 큰 수혜를 받을 것”이라고 전망했다.











![[컬처콕 플러스] '아파트' 대박난 로제, 제니·로사와 다른 점은?](https://img.etoday.co.kr/crop/320/200/2099568.jpg)