길리어드 “1년도 채 안돼 FDA 승인 믿기지 않아”
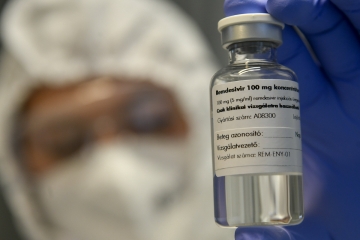
미국 식품의약국(FDA)이 제약사 길리어드사이언스의 '렘데시비르'를 신종 코로나바이러스 감염증(코로나19) 치료제로 정식 승인했다. 미국에서 코로나19 치료용으로 승인받은 최초이자 유일한 의약품이다.
22일(현지시간) CNBC 방송에 따르면 FDA는 이날 미국 생명공학기업 길리어드사이언스의 항바이러스제 렘데시비르를 코로나19 입원 환자에 사용할 수 있다는 정식 허가를 내줬다. 이에 따라 렘데시비르는 미국에서 정식으로 승인을 받은 첫 번째이자 유일한 코로나19 치료제가 됐다
이번 FDA의 정식 승인을 받아 렘데시비르는 앞으로 코로나19 입원 환자를 대상으로 한층 더 폭넓게 투여할 수 있게 됐다. FDA는 이번 승인에 대해 “입원이 필요한 코로나19 환자들 가운데 12세 이상, 체중이 최소 40kg 이상인 환자들에게만 사용할 수 있다”고 설명했다.
당초 에볼라 치료제로 개발된 정맥주사 형태의 렘데시비르는 코로나19 입원 환자를 상대로 한 임상시험에서 효과를 보이면서 주목을 받았고, FDA는 지난 5월 이 의약품에 긴급 사용 승인을 부여했다. 이후 렘데시비르는 다른 의약품들과 함께 코로나19 중증 입원환자들을 대상으로 보조 치료제로 활용돼왔다. 도널드 트럼프 대통령이 코로나19 진단을 받았을 때도 치료제 중 하나로 렘데시비르가 사용됐다.
이달 초 미국 국립알레르기 및 감염병연구소(NIAID)가 주도해 수행한 임상시험에서는 렘데시비르를 투여한 환자의 회복기간이 그렇지 않은 환자보다 5일 더 단축된 것으로 나타나면서 다시 한번 유효성이 확인되기도 했다. 길리어드는 이달 8일 코로나19 환자 1062명을 대상으로 한 임상시험 결과에서 렘데시비르를 투여받은 환자의 회복기간이 위약을 사용한 집단보다 5일 더 빨랐다고 밝혔다. 해당 연구결과는 국제학술지 ‘뉴잉글랜드의학저널(NEJM)’에도 발표됐다.
대니얼 오데이 길리어드 최고경영자(CEO)는 성명을 통해 “코로나19 팬데믹(세계적 대유행)이 발발한 이후부터 길리어드는 전 세계적인 보건 위기의 해법을 찾는 데 도움을 주기 위해 끊임없이 노력했다”며 “1년도 되지 않아 미국에서 이 약이 필요한 모든 환자에게 사용 가능하다는 FDA 승인을 얻게 됐다는 사실이 믿기지 않는다”고 말했다.
현재 길리어드는 향후 렘데시비르의 수요가 급증할 것으로 전망하고, 생산량 확대에 총력을 다하고 있다. 이 회사는 지난 8월 올해 연말까지 200만 명 이상의 투여분을 생산하고, 내년에는 수백만 회분을 추가로 더 만들어낼 계획이라고 밝힌 바 있다. 현재 길리어드는 이달 말까지 렘데시비르의 생산량이 글로벌 수요를 맞출 수 있을 것으로 기대하고 있다.
다만 렘데시비르는 이달 중순 렘데시비르가 코로나19 환자에 미치는 효과가 거의 없다는 세계보건기구(WHO)의 연구 결과가 나오면서 효과성을 둘러싼 논란이 일기도 했다. WHO가 입원 환자 1만1266명을 대상으로 진행하고 있는 ‘연대 실험’에서 렘데시비르가 환자의 입원 기간을 단축하거나, 사망률을 낮추지 못했다는 소식이 전해진 것이다.
당시 길리어드 측은 “WHO의 연대 실험 결과는 동료 검토 전에 공개된 것으로 알고 있다”며 “이번 실험은 렘데시비르의 효능을 검증하기 위해 실시된 무작위 표본을 대상으로 한, 강력한 증거를 바탕으로 한 임상 연구와 일치하지 않는다”고 반박했다.










![[정치대학] 美 대선, 막판까지 초박빙…당선자별 韓 영향은?](https://img.etoday.co.kr/crop/320/200/2098110.jpg)