SK㈜는 SK바이오팜이 개발한 수면 장애 치료 신약(SKL-N05)이 미국에서 임상3상 시험을 시작한다고 1일 밝혔다. SK바이오팜은 SK㈜가 100% 지분을 보유한 자회사이자 신약 개발 전문 회사다.
이번 3상은 SK바이오팜의 신약 개발 파트너인 미국 재즈사가 기면증 및 수면무호흡증으로 인한 주간 졸림증 환자를 대상으로 북미·유럽 지역 전문 병원에서 진행한다. 재즈사는 수면장애 분야 세계 최대 제약사다.
SK㈜는 수면 장애 치료 신약을 독자 개발한 뒤 우수한 약효 및 안전성을 확인했고, 2011년 재즈사에 글로벌 시장에 대한 기술 라이센스를 수출한 바 있다. 재즈사는 2017년까지 임상 3상 시험을 완료한 후 미국 식품 의약품국(FDA)의 판매 허가를 거쳐 2018년 신약을 시판할 계획이다.
SK㈜는 기술 수출 계약에 따라 재즈사로부터 임상 시험 단계별 기술료를 받을 뿐 아니라 시판 이후 매출액에 따른 로열티 수입을 올리게 된다. 또, 한국·일본·중국 등 아시아 주요 12개국 시장에 대한 판권을 보유하고 있어 신약 출시 후에는 아시아 시장에서 직접 마케팅을 진행할 예정이다.
기면증과 수면무호흡증 등으로 서양인의 15%가 일주일의 3일 이상 주간 졸림증을 경험하는 것으로 알려져 있으며, 수면장애 관련 신약 시장 규모는 30억 달러(약 3조원) 규모로 연평균 6% 이상 성장하고 있다.
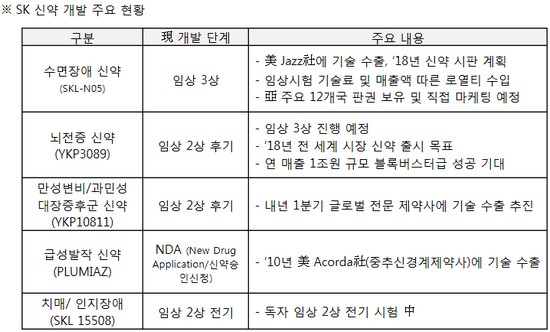
SK㈜ 조대식 사장은 “이번 수면 장애 신약 임상3상 외에도 SK바이오팜을 통해 자체 개발 중인 뇌전증(간질), 만성변비·과민성대장증후군 신약 등 경쟁력이 탁월한 신약 후보 물질을 확보하고 있다”며 “앞으로도 글로벌 시장을 대상으로 혁신적인 신약 개발에 매진할 것”이라고 말했다.
한편 SK㈜가 추진해온 신약 개발 사업은 성공 시 고수익이 기대되는 대신 장기간의 투자가 필요한 분야로, 1993년 신약 개발 시작 이후 글로벌 시장 진출을 목표로 중추신경계 질환 신약 개발에 집중해 왔다. SK바이오팜은 국내 최다인 15개 신약후보 물질의 임상 시험 승인(IND)을 미국 식품의약국(FDA)으로부터 확보한 바 있다.
특히, 현재 SK㈜가 독자적으로 임상을 진행하고 있는 뇌전증 신약(YKP3089)은 경쟁약물 대비 약효 및 안전성이 탁월한 것으로 평가 받았으며, 6월 임상 2상 후기 시험을 완료한 뒤 10월 경 임상 3상 시험을 진행할 예정이다. 2018년 미국을 포함한 글로벌 시장 출시를 목표로 하고 있으며, 현재 뇌전증 시장 1위 제품인 빔팻의 매출 규모를 고려하면 연 매출 1조원 이상의 블록버스터급 약물이 될 것으로 기대되고 있다.
이와 함께 만성변비·과민성대장증후군 신약(YKP10811)도 미국·한국에서 임상 2상 시험을 마무리 중에 있으며, 글로벌 전문 제약사와의 전략적 제휴를 통해 내년 1분기 기술 수출이 기대된다.
이에 업계에서는 오는 8월 통합지주회사 출범을 앞두고 SK바이오팜을 중심으로 한 신약 개발 사업이 통합 법인의 가치 제고에 중요한 축을 담당할 것으로 전망하고 있다.











![[컬처콕 플러스] '아파트' 대박난 로제, 제니·로사와 다른 점은?](https://img.etoday.co.kr/crop/320/200/2099568.jpg)