FDA, 관절염 치료제 바리스티닙과 동시 복용 긴급 승인
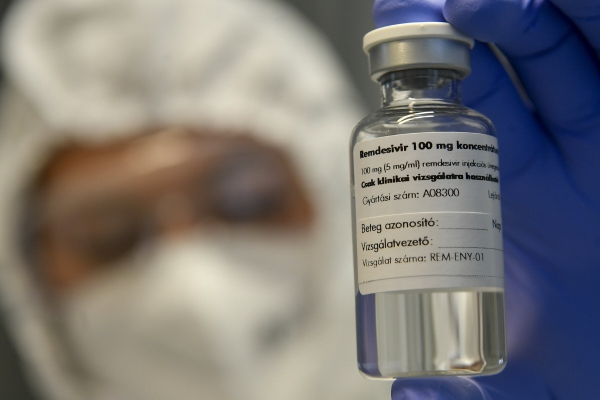
19일(현지시간) 미국 CNBC방송에 따르면 WHO 지침개발그룹(GDG)의 전문가 패널은 이날 길리어드사이언스가 개발한 렘데시비르를 코로나19 입원 환자에게 사용하는 것을 추천하지 않는다고 밝혔다.
패널은 “코로나로 입원한 환자 7000여 명을 대상으로 실시한 4개의 국제 임상시험 데이터를 포함해 여러 약물의 치료 효과를 비교한 새로운 데이터를 바탕으로 이번 권고를 했다”며 “증거를 철저히 검토해 렘데시비르가 환자 사망률이나 인공호흡기 필요성, 임상적으로 증상 호전에 필요한 시간 등 기타 중요한 결과에 의미 있는 영향을 미치지 않는다는 결론을 내렸다”고 설명했다.
다만 패널은 “렘데시비르를 계속해서 GDG의 효능 평가 실험에 등록해두는 것을 지지한다”고 덧붙였다.
앞서 WHO는 지난달 16일 “코로나19 치료제 후보군에 대한 연대 실험 중간 결과 렘데시비르가 환자 입원 기간과 사망률을 줄이는 데 거의 효과가 없다”고 밝혔다.
렘데시비르를 개발한 길리어드사이언스는 이날 이메일 성명에서 “렘데시비르는 코로나19 입원 환자 표준 치료법으로 미국과 일본, 영국, 독일 등 많은 국가의 믿을 수 있는 기관들로부터 인정받고 있다”며 “약 50개국에서 의사들이 코로나 환자를 위한 최초이자 유일하게 승인된 베클러리(Veklury·렘데시비르의 브랜드명)에 의존하는 이 시기에 WHO가 증거를 무시하는 것으로 보이는 지침을 내린 것에 실망했다”고 반박했다.
반면 FDA는 지난 5월 렘데시비르를 코로나19 치료제로 긴급사용 승인한 데 이어 지난달 22일에는 아예 코로나19 입원 환자들과 12세 이상 소아 환자를 대상으로 이 약을 정식 승인했다. 현재 렘데시비르는 코로나19 치료제로 미국에서 처음이자 유일하게 정식 승인을 받은 약품이다.
FDA는 이날 미국 제약업체 일라이릴리의 관절염 치료제 ‘바리스티닙’을 코로나19 치료 목적으로 렘데시비르와 함께 사용하는 것에 대해 긴급사용 승인을 내렸다. 산소 공급이 필요한 성인 입원 환자와 2살 이상의 어린이에 대해 동시 복용할 수 있다.
미국 국립알레르기·전염병연구소(NIAID) 지원을 받은 임상시험에 따르면 렘데시비르만 투약한 환자에 비해 두 약을 동시 처방한 환자는 평균 회복 기간이 하루 정도 줄었다.










![[정치대학] 美 대선, 막판까지 초박빙…당선자별 韓 영향은?](https://img.etoday.co.kr/crop/320/200/2098110.jpg)